(6分)下图是甲、乙两种固体物质的溶解度曲线。
(1)30℃时,甲的溶解度22乙的溶解度(填大于、等于或小于);

萃取操作的溶解度曲线将三角形内部分为两个区域,萃取操作在()进行
A、单相区
B、气相区
C、液相区
D、两相区
在溶解曲线以下的两相区,随温度的升高,溶解度曲线范围会(),萃取效果()。
A、缩小;越差
B、不变;不变
C、扩大;越好
D、缩小及扩大;不能确定
根据图中A、B、C、D四种物质的溶解度曲线,确定最适宜用结晶方法来分离的混合物是()
AA和B
BA和C
CB和D
DC和D
25℃时醋酸(A)–庚醇-3(B)–水(S)的平衡数据如本题附表所示。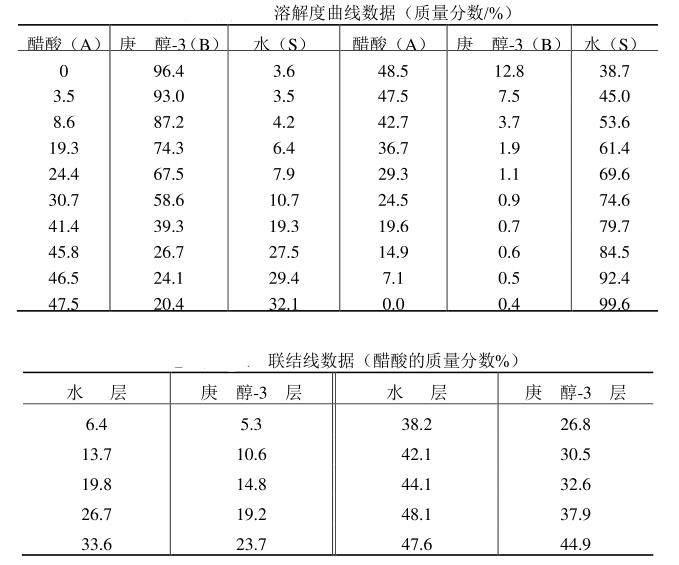 试求在直角三角形相图上绘出溶解度曲线及辅助曲线,在直角坐标图上绘出分配曲线。
试求在直角三角形相图上绘出溶解度曲线及辅助曲线,在直角坐标图上绘出分配曲线。
(8分)右下图是甲、乙、丙三种固体物质的溶解度曲线,请根据图示填空:
(1)随着温度的升高其溶解度反而减小的是_______;
在______℃时,甲与丙的溶解度相等。

A.A,B,C
B.C,B,A
C.C,A,B
D.A,C,B
关于下列四个图象的说法正确的是()
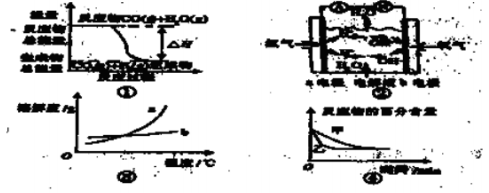


A.t1,t2,t3
B.t1,t3,t2
C.t3,t2,t1
D.t2,t1,t3
下列对溶解或结晶叙述正确的是()
A、溶液一旦达到饱和,就能自发地析出晶体
B、过饱和溶液的温度与饱和溶液的温度差称为过饱和度
C、过饱和溶液可通过冷却饱和溶液来制备
D、对一定的溶液和溶剂,其超溶解度曲线只有一条
1926年,我国著名化学家侯德榜先生创立了一种高效环保的纯碱生产方法“联合制碱法”,又称侯氏制碱法.其生产过程中有下列反应:
①NH3+CO2+H2O+NaCl=NH4Cl+NaHCO3②2NaHCO3=Na2CO3+H2O+CO2↑
(1)在反应①中,生成的氯化铵和碳酸氢钠的质量比是53.5:______.
(2)如图为碳酸氢钠和氯化铵的溶解度曲线,30℃时,碳酸氢钠饱和溶液中的溶质质量分数______(填“大于”、“等于”或“小于”)氯化铵饱和溶液中的溶质质量分数.
(3)氨盐水吸收CO2后生成了碳酸氢钠和氯化铵,请你根据溶解度曲线和生成物质量关系分析:为何碳酸氢钠首先结晶析出?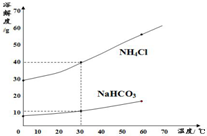
某混合液含溶质A30%(质量%,下同)原溶剂B70%,用纯溶剂S进行单级萃取,要求萃余液中A的浓度不超过10%,此时A组分的分配系数kA=1.5。试求: 1.所需溶剂比; 2.所得萃取液中A的浓度; 3.过程的选择性系数。 物系的溶解度曲线如图所示。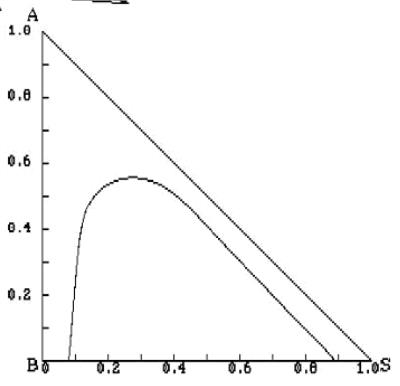
下图为氯化铵和硫酸钠的溶解度曲线。下列说法中不正确的是()
A30℃时,氯化铵、硫酸钠的溶解度相同
B氯化铵的溶解度随温度的升高而增大
C将50℃时硫酸钠的饱和溶液降低温度,始终有晶体析出
D将60℃时硫酸钠的饱和溶液降温至40℃,溶质的质量分数不变
A.E=607kg,R=393kg
B.E=393kg,R=607kg
C.E=500kg,R=500kg
D.E=460kg,R=540kg