
已知碱式碳酸铜[Cu2(OH)2CO3]受热易分解、能与酸反应。孔雀石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物。某学校化学研究小组以孔雀石为原料制备CuSO4·5H2O的流程如下:

请回答下列问题:(1)流程中,X的化学式是 ;由溶液B获得CuSO4·5H2O,需要经过加热蒸发、 、过滤等操作。(2)若通过置换反应由溶液B制备金属铜,反应的化学方程式是 。若选用下列物质与氧化铜反应制备铜,写出反应的化学方程式:①选用非金属单质 :②选用氧化物 。(3)工业上用焦炭在高温电炉中还原SiO2:可得到含有少量杂质的Si和CO,反应的化学方程式是 ,该反应类型为 。
(4分)2013环太湖国际公路自行车赛11月2日在江苏无锡著名风景区蠡湖之光开赛,来自五大洲的20支车队的120名职业选手“逐”梦江南。若某运动员和车总质量为100Kg,自行车在一段平直赛道上匀速行驶过程中受到的阻力为总重的0.05倍,1min通过了900m的路程,g取10N/kg,求:
(1)在这段赛道骑行过程中,该运动员克服阻力做了多少功;
(2)在这段赛道骑行过程中,该运动员做功的功率多大。
某研究性学习小组学习了工业“侯氏制碱法”的原理后,知道: NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl 。 【提出问题】能否在实验室模拟“侯氏制碱法”中制取NaHCO3的过程呢? 【实验验证】如图是该学习小组进行模拟实验时所用到的部分主要装置。已知浓氨水遇生石灰会产生大量的NH3。
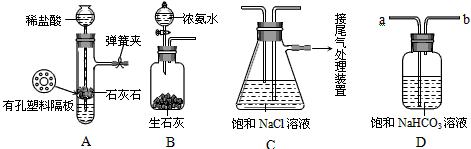
请回答下列问题: ⑴ 检验A装置气密性的方法是:塞紧带长颈漏斗的橡胶塞,夹紧弹簧夹后,从漏斗注入一定量的水,使漏斗内的水面高于试管内的水面,停止加水后,若 ,说明装置不漏气。 ⑵ D是连接在装置A与装置C之间的气体净化装置,进气口是 (填a或b),D的作用是除去______气体。 ⑶ 实验时先向饱和NaCl溶液中通入较多的NH3(溶液显碱性),再通入足量的CO2,其原因是______。(填写序号) ① 使CO2更易被吸收 ② NH3比CO2更易制取 ③ CO2的密度比NH3大 ⑷ 用________的方法将生成的NaHCO3晶体从混合物中分离出来。 【得出结论】利用“侯氏制碱法”在实验室可以制取NaHCO3。
作为推行“低碳经济”的重要科技进步,太阳能光伏发电成为2010年上海世博会的“亮点”。太阳能光伏发电最关键的材料是高纯硅。三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法。生产流程示意图如下:

(1)三氯甲硅烷(SiHCl3)是由 种元素组成的混合物。(2)“精馏”也是蒸馏的一种形式。通过蒸馏可把液体混合物分离开,原理是利用混合物各成分的 (填“熔点”或“沸点”)不同。(3)写出从粗硅到SiHCl3(粗)的化学方程式 。(4)为了达到绿色化学和资源综合利用的目的,上述生产流程中某些物质可循环使用,这些物质是 (填化学式)。(5)石英砂的主要成分是SiO2,含有少量Al2O3。若要除去石英砂中少量的杂质,可选用的试剂是 (填化学式)。
下列物质间转化,能一步实现的是
[ ]
A.C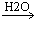 H2CO3 B.Fe2O3
H2CO3 B.Fe2O3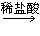 FeCl2 C.CuO
FeCl2 C.CuO CuSO4 D.Mg(OH)2
CuSO4 D.Mg(OH)2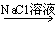 NaOH
NaOH